Flusso di energia
La vita sulla Terra dipende dal
continuo flusso di energia proveniente dal Sole. La quantità di energia
fornita dal Sole alla Terra è di circa
![]() calorie annue. È una quantità difficile da immaginare; per
esempio la quantità di energia solare che colpisce ogni giorno la Terra è più
o meno di due miliardi di volte superiore all’energia elettrica prodotta ogni
anno in Europa.
calorie annue. È una quantità difficile da immaginare; per
esempio la quantità di energia solare che colpisce ogni giorno la Terra è più
o meno di due miliardi di volte superiore all’energia elettrica prodotta ogni
anno in Europa.
Circa il 30% di questa energia solare è riflessa nello spazio sotto forma di luce, mentre un 20% circa viene assorbito dall’atmosfera (vedi figura). Gran parte del restante 50% di energia che raggiunge la superficie terrestre viene assorbita e convertita in calore; tuttavia, una piccola parte, inferiore all’1%, viene trasformata, attraverso una serie di operazione effettuate dalle cellule delle piante e di altri organismi fotosintetici, in glucosio e ATP, molecole che racchiudono nei loro legami l’energia che sostiene tutti i processi vitali. I sistemi viventi trasformano l’energia da una forma a un’altra, convertendo l’energia radiante del Sole nell’energia chimica e meccanica utilizzata da tutto ciò che è vivente. Questo flusso di energia è l’essenza della vita. Le cellule possono essere meglio comprese se le si considera come un sistema complesso atto a trasformare energia. All’altra estremità della scala biologica troviamo che la struttura di un ecosistema (cioè, l’insieme di tutti gli organismi viventi di un particolare luogo e dei fattori non viventi con cui essi interagiscono) o della biosfera stessa è determinata dagli scambi di energia che avvengono tra i gruppi di organismi presenti all’interno di essa.
Le leggi della termodinamica
“Energia” è oggi una parola così comune che sorprende sapere che il termine è stato coniato circa 200 anni fa, ai tempi dell’invenzione della macchina a vapore. Fu solo allora che gli scienziati e gli ingegneri cominciarono a comprendere che calore, movimento, luce, elettricità e le forze che tengono uniti gli atomi nelle molecole sono tutte forme diverse di energia, che può essere definita più semplicemente come la capacità di provocare un cambiamento, o, come si dice spesso, di compiere un lavoro. Questa nuova conoscenza portò allo studio della termodinamica, la scienza delle trasformazioni dell’energia, e alla formulazione delle sue leggi.
La prima legge
La prima legge della termodinamica afferma, molto semplicemente, che l’energia può essere trasformata da una forma all’altra, ma non può essere né creata né distrutta.
L’elettricità è una forma di energia, come la luce. L’energia elettrica può essere trasformata in energia luminosa (per esempio, facendo passare un flusso di corrente attraverso il filamento di tungsteno di una lampadina), e l’energia luminosa può a sua volta generare un flusso di elettroni (cioè una forma di energia elettrica), come avviene nella prima tappa della fotosintesi.
L’energia può essere accumulata in diverse forme e poi trasformata in altre ancora. Nei motori delle automobili, per esempio, l’energia accumulata nei legami chimici della benzina viene trasformata in calore (energia cinetica molecolare), che è poi, in parte, convertito nei movimenti meccanici degli ingranaggi del motore; parte dell’energia è ritrasformata in calore dall’attrito delle componenti del motore in movimento e parte esce dal motore con i prodotti di scarico. Analogamente, quando un organismo demolisce i carboidrati, trasforma l’energia accumulata nei legami chimici in altre forme. Nelle notti d’estate, per esempio, le lucciole trasformano l’energia chimica in energia meccanica, in calore, in lampi di luce e in impulsi elettrici che viaggiano lungo i nervi del corpo. Gli uccelli e i mammiferi trasformano l’energia chimica in calore necessario per mantenere costante la temperatura del loro corpo, e anche in energia meccanica nel movimento muscolare, elettrica nella trasmissione dell’impulso nervoso e in altre forme di energia chimica. Secondo la prima legge della termodinamica, in queste trasformazioni di energia (così come in tutte le altre) l’energia no è né creata né distrutta.
In tutte le trasformazioni energetiche, tuttavia, una parte dell’energia utilizzabile viene convertita in calore e dissipata come tale. Nel motore di un automobile, infatti, il calore prodotto dall’attrito e perduto nei prodotti di scarico, a differenza del calore rimesto nel motore stesso, non può compiere un lavoro, cioè non può spingere i pistoni e azionare gli ingranaggi in quanto viene dissipato nell’ambiente. Ciò nondimeno, esso fa parte della reazione complessiva. In un motore a benzina circa il 75% dell’energia presente in origine nel carburante viene trasferita nell’ambiente sotto forma di calore, cioè viene convertita in un aumento del movimento di atomi e molecole dell’aria. Nello stesso modo, il calore prodotto dai processi metabolici degli animali è dissipato nell’aria o nell’acqua circostante.
Perciò la prima legge della termodinamica può anche essere enunciata come segue: in tutti gli scambi e in tutte le trasformazioni energetiche, l’energia complessiva del sistema e dell’ambiente circostante, dopo la trasformazione, è uguale all’energia complessiva presente prima che la trasformazione abbia luogo. Un “sistema” può anche essere un’entità ben definita come, per esempio, un candelotto di dinamite, un motore di un automobile che gira a folle, un mitocondrio, una cellula, una foresta o la terra stessa. “L’ambiente circostante” è tutto ciò che sta al di fuori del sistema.
La seconda legge
L’energia dissipata come calore in una trasformazione energetica non è andata distrutta (infatti, è ancora presente nel movimento casuale di atomi e molecole), ma è stata “perduta” per ogni scopo pratico e quindi no è più disponibile per compiere un lavoro utile. Questo ci porta alla seconda legge della termodinamica, più interessante dal punto di vista biologico.
La seconda legge afferma che in tutte le trasformazioni e scambi energetici, se il sistema in questione non cede o acquista energia, l’energia potenziale presente alla fine sarà sempre minore dell’energia potenziale presente all’inizio. Questa legge è del tutto in armonia con l’esperienza quotidiana: un ammasso rotolerà giù da una collina, ma mai verso l’alto, o una palla, cadendo, rimbalzerà, ma non fino a raggiungere l’altezza dalla quale è caduta.
Un processo fisico o chimico
che presenta, nello stadio finale, un’energia potenziale minore di quella
presente nello stadio iniziale, è un processo che libera energia e viene detto esoergonico. Solo le reazioni
esoergoniche possono avvenire spontaneamente, cioè senza che il sistema prenda
energia dall’esterno. Al contrario, un processo in cui l’energia potenziale,
alla fine, è maggiore di quella presente all’inizio, è un processo che
richiede energia: esso viene detto endoergonico e, perché possa avvenire, il
sistema deve ricevere un apporto energetico.
processo che libera energia e viene detto esoergonico. Solo le reazioni
esoergoniche possono avvenire spontaneamente, cioè senza che il sistema prenda
energia dall’esterno. Al contrario, un processo in cui l’energia potenziale,
alla fine, è maggiore di quella presente all’inizio, è un processo che
richiede energia: esso viene detto endoergonico e, perché possa avvenire, il
sistema deve ricevere un apporto energetico.
Le molecole contengono energia
potenziale immagazzinata nei legami chimici che tengono uniti tra loro gli
atomi. Quando, durante una reazione chimica, questi legami si spezzano,
l’energia in essi contenuta può essere utilizzata per formare nuovi legami
chimici o essere liberata sottoforma di calore. Se l’energia potenziale dei
prodotti è minore di quella dei reagenti, la reazione è esoergonica e verrà
liberata energia; se, invece l’energia potenziale dei prodotti è maggiore di
quella dei reagenti, la reazione è endoergonica e avverrà solo grazie ad un
apporto di energia.
Un altro fattore che determina la differenza di energia potenziale tra reagenti e prodotti di una reazione chimica è il grado di disordine dei reagenti e dei prodotti: maggiore è il disordine, minore risulta l’energia potenziale. Pertanto, la seconda legge della termodinamica può essere enunciata anche in un altro semplice modo: tutti i processi naturali tendono sempre a far aumentare il disordine dell’Universo. Questo disordine è detto entropia. Nella figura vedete l’esempio di come può essere dissipata una forma concentrata di energia. In natura i processi tendono verso la casualità o il disordine. Soltanto un apporto di energia può invertire questa tendenza e ripristinare lo stato iniziale a partire da quello finale; alla fine, comunque, prevarrà il disordine, perché la quantità totale di energia nell’Universo è una quantità finita.
I sistemi viventi e la seconda legge
L’Universo, secondo il modello attuale, è un sistema chiuso, cioè né la materia né l’energia possono entrare o uscire dal sistema. La materia e l’energia presenti nell’Universo al momento del Big Bang costituiscono tutta la materia e l’energia che si potrà mai vivere. Inoltre, dopo ogni trasformazione e ogni scambio di energia, l’Universo nel suo insieme ha meno energia potenziale e più entropia di prima. Da questo punto di vista l’Universo si sta esaurendo; le stelle si spegneranno con un tremolio, una alla volta, e la vita, ogni forma di vita su ogni pianeta, cesserà. Alla fine cesserà anche il movimento di ogni singola molecola. Tuttavia, anche lo scienziato più pessimista crede che questo non accadrà prima di 20 miliardi di anni.
Nel
frattempo la vita può esistere proprio grazie al fatto che l’Universo
 si
sta esaurendo. Anche se l’Universo, nel suo insieme, è un sistema chiuso, la
Terra non lo è; essa infatti, come abbiamo visto, riceve dal Sole un apporto
di energia di circa
si
sta esaurendo. Anche se l’Universo, nel suo insieme, è un sistema chiuso, la
Terra non lo è; essa infatti, come abbiamo visto, riceve dal Sole un apporto
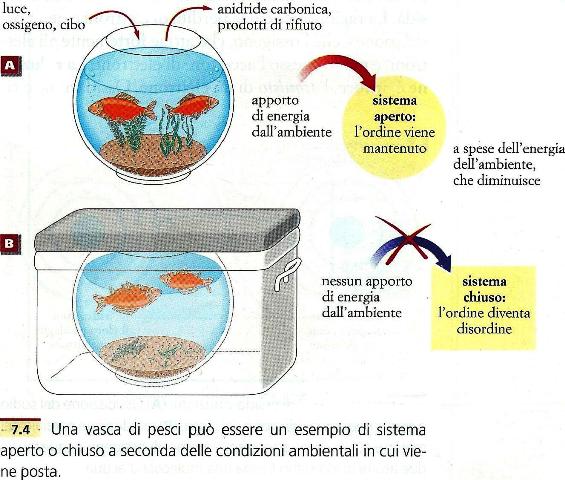
di energia di circa![]() calorie all’anno. La figura mette a confronto un sistema
aperto (come può essere appunto il nostro pianeta) con un sistema chiuso: una
vasca per i pesci (A) è un sistema aperto in cui un
apporto costante di energia dall’esterno mantiene l’ordine; la stessa vasca
per i pasci posta al buio in un contenitore sigillato (B) diventa un
sistema chiuso in quanto né materia né energia possono entrare o uscire da
esso e le eventuali forme di vita spariranno.
calorie all’anno. La figura mette a confronto un sistema
aperto (come può essere appunto il nostro pianeta) con un sistema chiuso: una
vasca per i pesci (A) è un sistema aperto in cui un
apporto costante di energia dall’esterno mantiene l’ordine; la stessa vasca
per i pasci posta al buio in un contenitore sigillato (B) diventa un
sistema chiuso in quanto né materia né energia possono entrare o uscire da
esso e le eventuali forme di vita spariranno.
Gli organismi fotosintetici sono degli specialisti nel catturare l’energia luminosa liberata dal Sole mentre esso si consuma. Questi organismi utilizzano l’energia per organizzare molecole piccole e semplici (acqua e anidride carbonica) in molecole più grosse e complesse (zuccheri). In questo processo l’energia luminosa catturata viene accumulata come energia chimica nei legami chimici presenti negli zuccheri e in altre molecole.
Le cellule, comprese quelle fotosintetiche, possono trasformare questa energia accumulata in movimento, elettricità, luce e, trasferendo l’energia da un tipo di legame chimico ad un altro, in forme più utili di energia chimica. A ogni trasformazione parte dell’energia è perduta nell’ambiente sotto forma di calore; ma prima che l’energia catturata dal Sole sia completamente dissipata, gli organismi la usano per creare e mantenere la complessa organizzazione delle strutture e delle attività che costituiscono la vita.